Skeppsvrak i fara: vetenskapen kommer till undsättning! Understand article
Översättning: Magnus Sandström. Mary Rose är ett av flera berömda historiska skepp som bärgats under de senaste decennierna. På grund av de syrefattiga förhållandena på havsbotten kan skeppsvrak bevaras rätt väl. Montserrat Capellas och Dominique Cornuéjols från the European…
Mary Rose

Roses skrov återstår efter att
ha legat begravt på
avsbotten i 437 år
Foto med tillstånd av © the
Mary Rose Trust
Mary Rose, den engelska Tudorkungens Henry VIII flaggskepp, är det enda 1500-talsskepp i världen som visas för publik. Byggd i Portsmouth och sjösatt 1511 var Mary Rose Tudor-flottans stolthet i 34 år, till kriget med Frankrike 1545. Orsaken till förlisningen är oklar, men oskicklig manövrering tycks vara det mest sannolika skälet. Oavsett orsaken, när skeppet fick slagsida och vattnet forsade in genom de öppna kanonportarna var hennes, tillika med de hundratals besättningsmännens, öde beseglat. I över 400 år låg hon på 14 meters djup, begravd i lera på havsbotten vid Englands sydkust, tills marinarkeologer bärgade vraket 1982. Skeppet med dess tusentals föremål ger en sällsynt inblick i livet till sjöss på Tudortiden, men bevarandet kräver omsorgsfull konservering.
Problemen med svavel- och järnföreningar
Svavelföreningar som ansamlats i skeppets trästruktur utgör det huvudsakliga hotet mot det bärgade vraket av Mary Rose.
När bakterier i syrefattigt havsvatten bryter ned organiskt avfall, t.ex. kolhydrater, (CH2O)n, reduceras samtidigt sulfatjoner, SO42-, till svavelväte, H2S.
(CH2O)n + n/2SO42- → n/2H2S(aq) + nHCO3–
Svavelväte i vattenlösning, H2S(aq), tränger in i trä där det bildar fasta reducerade svavelföreningar, t ex tioler R-SH (R betecknar en organisk del) i träets lignin, och dessutom järn(II)sulfider när järnjoner finns närvarande.
Under århundraden ackumulerades reducerade svavelföreningar; kemiska analyser visar att Mary Roses träskrov nu innehåller omkring 1% svavel (totalt 2 ton S). Så snart som skeppets skrov lämnade vattnet började svavelföreningarna i träet långsamt oxidera och bilda svavelsyra, H2SO4(aq). Om syran lämnas obehandlad riskerar man att cellulosafibrerna i träet kan brytas ned och därvid minska skrovets stabilitet.
I närvaro av järnjoner blir syrahotet särskilt akut eftersom järnjoner katalyserar oxidationsprocessen och därigenom påskyndar produktionen av svavelsyra. Mary Roses trä innehåller, liksom många andra skeppsvrak, järn från korroderade järnbultar, spikar och andra järnföremål på skeppet. På havsbotten har kombinationen lösta järn(II)joner och svavelväte gett upphov till järnsulfider, t ex pyrit FeS2, som är instabila när det fuktiga träet kommer i kontakt med syre:
FeS2(s) + 7/2O2 + (n+1)H2O → FeSO4·n(H2O)(s) + H2SO4(aq)
Utfällningar av de hydratiserade järn(II)sulfaterna melanterit, FeSO4·7(H2O)(s), och rozenit, FeSO4·4(H2O)(s), förekommer ofta på svavelrikt marinarkeologiskt trä.
Röntgenstrålning hjälper
Röntgenstrålning är känd för att ha medicinsk användning inom avbildning och radioterapi, men är också till nytta när ömtåliga skeppsvrak ska behandlas. Med röntgenstrålning kan man på ett icke-förstörande sätt analysera grundämnen i ett föremål och bestämma deras kemiska tillstånd. För att erhålla sådan detaljerad information för svavel väljer man lämpligen en metod som kallas röntgenabsorptionsspektroskopi. Röntgenstrålning med känd energi då får träffa provet så att en elektron i svavelatomen inre elektronskal exciteras till ett högre energitillstånd, eller skickas ut som en fotoelektron. Därefter kan man antingen mäta den kinetiska energin hos dessa fotoelektroner (med en teknik som kallas fotoelektronspektroskopi), eller få ett mått på röntgenabsorptionen genom att mäta den röntgenstrålning som provet avger när den exciterade atomen återvänder till sitt normaltillstånd (röntgenfluorescens).
På detta sätt erhålls den exciterade elektronens bindningsenergi, som är karakteristisk för varje typ av svavelförening. För Mary Rose behövde man ta reda på svavel- och järnföreningarnas mängd och fördelning i träet. Mycket intensiv röntgenstrålning, i form av synkrotronljus (se box), var då nödvändig för att i detalj ta reda på den kemiska sammansättningen och dra slutsatser om det bästa sättet att förhindra ytterligare nedbrytning.
Ny konserveringsteknik

under de senaste tio åren
spraybehandlats med en
polyetylenglykollösning som
ersätter vattnet och
förhindrar sprickbildning när
träet torka
Foto med tillstånd av © the
Mary Rose Trust
För att långsiktigt kunna bevara Mary Roseär det nödvändigt att avlägsna järnsulfiderna, de svavelföreningar som snabbast bildar syra, från träet. Under den pågående konserveringsbehandlingen, som påbörjades för tio år sedan, spolas syran bort i takt med att den bildas (se foto). För att snabbare göra sig av med de syrabildande järnsulfiderna under spraybehandlingen skulle man kunna testa mild oxidation med singlettsyre, 1O2 (kortlivade energirika syremolekyler, som bildas vid UV-bestrålning genom att excitera en valenselekton i en vanlig O2-molekyl). Ett annat sätt att öka reaktionshastigheten är en måttlig höjning av temperaturen på spraylösningen, vilket dock kan innebära en hälsorisk genom att Legionella-bakterier kan bildas.
Nyligen utförda röntgenmikroskopianalyser vid den europeiska synkrotronstrålningsanläggningen gav forskarna möjlighet att föreslå ytterligare åtgärder. I en metod som håller på att testas avlägsnar man järn med hjälp av en komplexbildande förening, ett kelat kallat EDMA (etylendiiminobis(2-hydroxy-4-metyl-fenyl) ättiksyra). EDMA binder järn(III)joner mycket starkt och kan därigenom lösa upp järnföreningar. Även rost, FeOOH(s), bildar till och med i alkaliska lösningar vattenlösliga järnkomplex med EDMA och kan tvättas ur träet. När järnet är borta oxiderar återstoden av svavlet långsammare vilket kan kontrolleras med ett stabilt klimat och antioxidanter.
Framförallt är det viktigt att övervaka behandlingarnas effektivitet, och röntgenanalyser är ett effektivt sätt att uvärdera järnextraktionen och hur effektivt vissa typer av svavelföreningar avlägsnas.
Synkrotronröntgen
I en synkrotron accelereras elektroner tills de uppnår mycket hög energi (sex miljarder elektronvolt vid ESRF i Frankrike). Dessa högenergielektroner förs sedan in i en förvaringsring, där de cirkulerar i vacuum med nära ljushastighet. Synkrotronröntgenstrålning avges när elektronerna ändrar riktning i starka magnetfält och strålningen riktas mot de experimentstationer som omger ringen.
Röntgenstrålningen som produceras vid ESRF är tusen miljarder gånger starkare än den strålning som avges av sjukhusröntgeninstrument. Därför kan denna riktade och mycket intensiva synkrotronljusstrålning användas till att studera strukturen hos materia på en detaljnivå som är omöjlig att uppnå med standardröntgeninstrument. Synkrotronljuskällor kan därför liknas vid supermikroskop, med användning inom en mängd forskningsområden, t ex materialvetenskap, arkeologi, biologi och fysik.

belägenhet
Det finns för närvarande 70 synkrotroner i världen. Olika tekniker, alltifrån röntgendiffraktion och lågvinkelspridning till fotoelektronspektroskopi och röntgenabsorption på mikroskopnivå, finns där tillgängliga till allt fler forskare. Dessa tekniker används för att studera materia i olika former, som kristaller och polymerer, biologiska och miljörelaterade prover, fasta föreningar, vätskor och gaser.
Synkrotronröntgenstrålning är även användbar vid analys av historiska skeppsvrak, för att i mikroskopisk detalj kunna fastställa kvantitet, fördelning och kemiskt tillstånd för svavel- och järnföreningar. På detta sätt kan forskarna undersöka det marinarkeologiska träets tillstånd och förbättra konserveringsmetoderna.
I detta syfte har professor Magnus Sandström och hans forskargrupp från Stockholms universitet regelbundet sedan 2001 färdats till Stanforduniversitetets synkrotronstrålningslaboratorium, Stanford Synchrotron Radiation Laboratory SSRL, i Kalifornien, USA. De började med att ta reda på varför syra bildades i det svenska 1600-talsskeppet Vasas trä, och har nu utökat sin forskning till att omfatta även andra historiska skeppsvrak, såsom Mary Rose. Förra året kom de till ESRF för att göra undersökningar som kompletterar de som utförts i Stanford.
Extraktion av järnföreningar

sänks ned i en alkalisk
natrium-EDMA- lösning
löses järnföreningarna ut
från träet som det blodröda
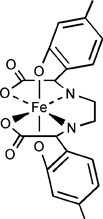
komplexet [FeIII(EDMA]-.
Foto av Stefan Evensen med
tillstånd av Statens maritima
museer, Sverige, © Stefan
Evensen
Forskarna undersökte det svenska regalskeppet Vasa, som sjönk på sin jungfruresa den 10 augusti 1628, och kom på idén att lösa upp järnföreningarna i träet och avlägsna dem som komplex i vattenlösning. Tester pågår nu med ett kelat (komplexbildare) som kallas EDMA. Natriumsaltet av det lösliga järnkomplexet, [FeIII(EDMA)]-, används i stora kvantiteter som ett järnmikronäringsämne för citrusträd, som inte kan ta upp järn från alkaliska jordar där vanliga järnföreningar är olösliga. Föreningen används som gödningsmedel i apelsinodlingar i Spanien och för citroner och druvor i Italien och Frankrike.
Förståelsefrågor
Magnus Sandström
- Både för Vasa och Mary Rose har analyser visat att deras träskrov innehåller omkring 2 ton av grundämnet svavel, S, i olika föreningar. Om 1000 kg svavel i träet förekommer i form av pyrit, FeS2, hur mycket svavelsyra, H2SO4(aq), skulle ha bildats när all pyrit oxiderat?
Två reaktionsvägar är vanliga: 1. till hydratiserat järn(II)sulfat:
FeS2(s) + 7/2O2 + (n+1)H2O → FeSO4·n(H2O)(s) + H2SO4(aq)
eller 2. till götit, a-FeOOH (rost):
FeS2(s) + 15/4O2 + 5/2H2O → FeOOH(s) + 2H2SO4(aq)
- Natriumvätekarbonat (natriumbikarbonat, NaHCO3) sätts då och då till Mary Roses återcirkulerande spraykonserveringslösning när det sjunkande pH-värdet behöver återställas till omkring 7. Hur mycket natriumvätekarbonat skulle behövas för att neutralisera den syra som kan bildas från oxiderad pyrit innehållande 1000 kg svavel (se fråga 1)?
- Kristallin pyrit, som har volymen 40 Å3 per FeS2-enhet (1 Å = 10-10 m), expanderar dramatiskt vid oxidation. Volymen per formelenhet av två kristallina produkter: de hydratiserade järn(II)sulfaten melanterit, FeSO4·7(H2O)(s), och rozenit, FeSO4·4(H2O)(s), är 243.5 Å3 resp, 162.7 Å3. Även natrojarosit, NaFe3(SO4)2(OH)6, med en volym av 266.0 Å3 per formelenhet, är vanligt förekommande på Vasa’s trä.
Uppskatta hur många gånger volymen kommer att öka när en pyritkristall oxiderar och de fasta föreningarna a) FeSO4·7(H2O)(s), b) FeSO4·4(H2O)(s) eller c) NaFe3(SO4)2(OH)6 kristalliserar som produkter. Vilka effekter skulle dessa processer kunna ha om de sker inuti trästrukturen? Vad är järnets oxidationstal i natrojarosit?
- Sök i en kemisk lärobok upp ett schematiskt diagram som visar molekylära orbitalenerginivåer för syremolekylen O2 i grundtillståndet. Förklara hur absorption av ljusenergi kan leda till att det bildas singlettsyre, 1O2, där alla elektroner bildat par.
Svar till förståelsefrågorna.
Resources
- Mary Rose kan beskådas i Mary Rose Museum, Portsmouth, Storbritannien. Information om skeppet, informationsblad samt besöksdetaljer finns tillgängliga på hemsidan: www.maryrose.org.
- Det välbevarade Vasaskeppet är utställt på Vasamuseet i Stockholm, Sverige. Detaljer om Vasas historia, pågående forskning kring hennes bevarande, samt besöksinformation finns på: www.vasamuseet.se.
- En beskrivning av arbetet i Sandströms forskargrupp med att bevara Vasa och Mary Rose finns på: www.fos.su.se/~magnuss/.
- ESRF (European Synchrotron Radiation Facility) är en internationell anläggning i Frankrike, som tillsammans med 18 andra länder, driver och utvecklar den mest kraftfulla synkrotronljuskällan i Europa. Mer än 5000 forskare kommer till ESRF varje år för att använda ljuskällan och dess instrument, se www.esrf.fr.
Institutions
Review
Denna artikel bör vara av stort intresse för lärare inom naturvetenskap, men också för historielärare. Den är användbar för lärare som vill införa fler kemi- och fysiktillämpningar i sin undervisning, och för att stimulera till konstruktiv användning av naturvetenskap i ovanliga situationer. Den skulle också kunna fungera som en inkörsport för mer erfarna studenter, som kan använda de informativa web-hänvisningarna till fortsatt forskning i andra vetenskapliga och historiska aspekter av denna artikel.
Jag uppskattade artikeln. Den stimulerade mig tillräckligt för att följa upp en del av den angivna informationen.
Tim Harrison, UK
