Nanotechnologie in der Schule Teach article
Übersetzt von Hildegard Kienzle-Pfeilsticker. Matthias Mallmann von NanoBioNet e.V. erklärt was Nanotechnologie wirklich ist und bietet zwei Nano-Experimente für den Unterricht an.
Nanotecnologie ist zum populären Modewort in Wissenschaft und Politik geworden. Diese Schlüsseltechnologie wird nicht nur für eine der größten Innovationsquellen für Technik, Medizin und andere Bereiche gehalten, sondern auch für eine der größten Herausforderungen für das 21. Jahrhundert. Die Technologie wird von europäischen Universitäten und Ausbildungsprogrammen auf hohem Level bereits ausgiebig abgedeckt. Obwohl der Begriff Nanotechnologie vielen High-School-Studenten geläufig ist, wird der Stoff in europäischen Schulen nicht flächendeckend unterrichtet. Dieser Artikel beschreibt mehrere Initiativen, die zum Ziel haben, bei europäischen Wissenschaftslehrenden die Nanotechnologie mehr ins Bewusstsein zu rücken, und er beschreibt zwei Experimente aus der Nanotechnologie, die für das Klassenzimmer geeignet sind.
Was ist Nanotechnologie?

Glasfenster, die mittels
Nanotechnologie gefärbt
wurden
Mit freundlicher Genehmigung
von NanoBioNet eV
Nanotechnologie ist nicht wirklich neu. Sie arbeitet mit Teilchen und Prozessen in der Größenordnung von 10-9 m (1 Nanometer), in der Dimension von Molekülen und Atomen – ein Maßstab mit dem Chemiker, Biochemiker und Zellbiologen schon seit Jahrhunderten arbeiten.
Im Nanobereich können sich die Materialeigenschaften ändern. Beispielsweise sind Härte, elektrische Leitfähigkeit, Farbe oder chemische Reaktivität winziger Materialpartikel vom Durchmesser abhängig. Spezifische Funktionalitäten können daher durch Verminderung der Partikelgröße auf 1-100 nm erreicht werden.
Eine wohlbekannte Anwendung früher Nanotechnologie ist die rubinrote Farbe, die für gefärbte Fenster im Mittelalter verwendet wurde (siehe Abbildung). Die Farbe resultiert von Goldatomen, die Cluster von Nanopartikeln anstatt der üblicheren, festen Form bilden. Diese kleinen Goldpartikel erlauben dem langwelligen Rotlicht den Durchtritt, blockieren aber das kurzwelligere blaue und gelbe Licht. Daher hängt die Farbe sowohl vom verwendeten chemischen Element (Gold) als auch von der Partikelgröße ab; Silberpartikel beispielsweise können gelbe Farbe ergeben.
Neu jedoch ist der multidisziplinäre Ansatz und die Möglichkeit, diese Teilchen zu „beobachten”. Das Rasterkraftmikroskop, das in den späten 1980er Jahren entwickelt wurde, ermöglicht den Wissenschaftlern, Strukturen im Nanometerbereich zu sehen und sogar mit einzelnen Atomen mitttels Rastersondenmikroskopie zu experimentieren. Heute sind Biologen in der Lage, mit Chemikern sterische Effekte von Zellmembranen zu diskutieren, während Physiker die Werkzeuge für die in vivo-Beobachtung liefern. Nanopartikel spielen eine wichtige Rolle in der Pharmaindustrie (indem sie Wirkstoffe an die Zielorte im Körper bringen), bei der Herstellung von Dispersionsfarbe und Kosmetika und bei der Optimierung von Katalysatoren. Daher hat die Nanotechnologie alle Naturwissenschaften zusammengeführt und schafft Verknüpfungen zwischen verschiedenen Disziplinen.
Initiativen für Schulen

Mit freundlicher Genehmigung von
Lehrstuhl für physikalische Chemie
, Universität des Saarlandes
Für Wissenschaftslehrer sind bereits einige Materialien erhältlich, um Studenten in die Nanotechnologie einzuführen. Allerdings werden die Materialien meist in der Landessprache veröffentlicht. Beispielsweise bietet die Saarlab Initiativew1Labortage für ganze Schulklassen an, während europäische Wissenschaftsmuseen und Wissenschaftszentrenw2 Ausstellungen über Nanotechnologie anbieten oder bringen, wie die deutsche Initiative nanoTruckw3, Interessierte dem Thema mit mobilen Ausstellungen näher, die für öffentliche Veranstaltungen gebucht werden können. Einige Universitäten, wie die University of Cambridgew4, bieten Schulbesuche, interaktive Vorlesungen, Seminare und Workshops an. Zusätzlich gibt es viele Quellen online, die Informationen, Filme und Spiele für Schüler und Studenten anbietenw5.
Um diese Lücke zu füllen, bietet NanoBioNet e.V.w6nicht nur Ausbildungskurse und Training für Lehrer an, sondern hat auch einen mehrsprachigen (deutsch, englisch und französisch) Experimentierkasten (die NanoSchoolBoxw7) für den Unterricht von Schülern in Nanotechnologie entwickelt. Einige der Experimente in der NanoSchoolBox eignen sich für Demonstrationen, andere können unter der Anleitung des Lehrers ohne viel Vorbereitung in praktische Übungen intergriert werden.
Der experimentelle Schul-Kit enthält 14 Versuche und fünf Darstellungen der folgenden Themen:
- Der Lotuseffekt und technische Anwendungen für Nanoschichten
- Funktionalität durch Nanotechnologie (verschiedene Effekte nanotechnologischer Beschichtungen wie Kratzfestigkeit, Feuerschutz und erhöhte elektrische Leitfähigkeit durch Indium-Zinn-Oxid)
- Die Verwendung von Titandioxid in der Nanotechnologie
- Ferrofluide
- Goldcluster im Nanomaßstab
Obwohl die Experimente vor allem für den Chemieunterricht gedacht sind, sind dank der interdisziplinären Struktur der Nanotechnologie manche von ihnen auch für den Physik- oder Biologieunterricht geeignet. Es folgen zwei Beispiele.
Ferrofluide

Zusammensetzung von
Ferrofluidpartikeln
Mit freundlicher Genehmigung von
NanoBioNet eV
Mit freundlicher Genehmigung
von NanoBioNet eV
Ferrofluide sind kolloidale Lösungen extrem kleiner Partikel (d. h. von Partikeln, die durch ein äußeres magnetisches Feld permanent magnetisiert werden können) wie Kobalt, Nickel oder Eisen, die in einem flüssigen Kohlenwasserstoff suspendiert sind. Die Partikel haben eine Oberfächenbeschichtung, die das Zusammenklumpen verhindert. Ferrofluide sind die einzigen magnetischen Materialien in flüssiger Form.
Die NanoSchoolBox enthält zum einen Ferrofluide zur Durchführung des Experiments und zum anderen Anweisungen zur Herstellung eigener Ferrofluide im Labor. Ferrofluide können auch von FerroTec GmbHw8 gekauft werden.
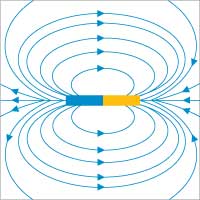
In diesem einfachen Experiment ordnen sich die ferromagnetischen Partikel entlang der magnetischen Feldlinien um einen Magneten an und machen so das magnetische Feld sichtbar.
Materialien
- Ferrofluid
- Leeres Glasröhrchen mit Crimp-Verschluss
- Tensidlösung (Oberflächenbeschichtung)
- Magnet
- Pipette
- Wasser
Vorgehen
- Das Glasröhrchen zu dreiviertel mit Wasser füllen und 2-5 Tropfen Tensidlösung zugeben (oberflächenaktive Substanz).
- Mit der Pipette vorsichtig ein paar Tropfen Ferrofluid zugeben. Es wird sich am Boden absetzen.
- Das Glasröhrchen dicht verschließen.
- Den Magneten dicht an das Ferrofluid halten.
Wenn sich die Partikel im magnetischen Feld ausrichten, bildet sich eine typische „Stachelschweinstruktur”, in der die Stacheln den magnetischen Feldlinien entsprechen (siehe die Bilder). Die Oberflächenspannung der Flüssigkeiten und die Schwerkraft wirken dem magnetischen Feld entgegen mit dem Ergebnis, dass die geordneten Strukturen in der Flüssigkeit als Reaktion auf die drei einwirkenden Kräfte gebildet werden.
- Versuchen Sie, das Ferrofluid mit Hilfe des Magneten durch das Wasser zu bewegen. Je nachdem ob der Magnet parallel oder senkrecht zur Oberfläche des Ferrofluids gehalten wird, ändert sich die Orientierung des magnetischen Feldes und folglich diejenige der Flüssigkeit.
- Schütteln Sie das Gläschen vorsichtig, um das Ferrofluid im Wasser zu verteilen. Da die Ferropartikel sich nicht lösen, setzen sie sich schließlich am Boden ab. Man kann diesen Vorgang mit Hilfe eines Magneten beschleunigen und dabei wunderschöne Effekte beobachten. Dazu ziehen Sie den Magneten mehrmals schnell über die Seite des Gläschens und erhalten so Streifen, Wolken und so weiter.



Mit freundlicher Genehmigung von NanoBioNet eV
Anmerkungen zur Sicherheit
- Ferrofluide müssen mit großer Sorgfalt und in reinem Milieu gehandhabt werden, da sie dauerhaft einfärben.
- Ein Labormantel, Handschuhe und Schutzbrille sind zu tragen. Bei Hautkontakt mit einem Ferrofluid ist die Stelle mit einer Seife zu waschen.
- Bewahren Sie Ferrofluide immer in einem verschlossenen Gefäß auf, um Verdampfung zu vermeiden.
- Die Ferrofluide und Materialien, die mit ihnen kontminiert sind, sollten wie Motoröl entsorgt werden (als Gefahrstoffe oder an einer Sammelstelle) und nicht in den Abguss gegossen werden.
Nanogold
Forscher machen sich die Licht absorbierende Eigenschaft von Goldpartikeln zunutze. Beispielsweise können Antikörper mit Goldpartikeln markiert werden. Im weißen Licht wird die rote Farbe der Metallpartikel sichtbar. Diesen Effekt macht man sich in manchen Schwangerschaftsselbsttests zunutze, bei denen Gold-Nanopartikel über den Teststreifen fein verteilt sind.
Der UltiMed®-Schwangerschaftstest beispielsweise beruht auf diesem Prinzip, um humanes Choriongonadotropin (hCG) nachzuweisen, das in der frühen Schwangerschaft vom befruchteten Ei und der Gebärschmutterschleimhaut abgegeben wird. hCG besteht aus zwei Untereinheiten: α und β. Auf dem Teststreifen sind α-Untereinheiten von hCG immobilisiert, die eine rote Linie bilden, wenn eine Schwangerschaft besteht. An anderer Stelle auf dem Streifen befinden sich mit kolloidalen Goldpartikeln markierte Anitkörper, die spezifisch für die β-Untereinheit von hCG sind.
Mit freundlicher Genehmigung von
kimkole / iStockphoto
Wird der Streifen in Urin getaucht, können die markierten Goldpartikel wegen der Flüssigkeit im Streifen mittels Kapillarkräften wandern. Enthält der Urin hCG (d.h. die Frau ist schwanger), binden die β-Untereinheiten von hCG an die markierten Goldpartikel. Wenn die an das Gold gebundenen die immobilisierten α-Untereinheiten erreichen, verbinden sich die α- und β-Untereinheiten und bilden einen Gold-hCG-Komplex. Ist die hCG-Konzentration hoch genug, wird der Komplex als rote Linie sichtbar und zeigt an, dass die Frau schwanger ist. Weitere Goldpartikel binden an eine zweite Linie und zeigen an (egal ob positiv oder negativ), dass der Test ordnungsgemäß durchgeführt wurde.
Im folgenden Experiment werden wir Goldcluster im Nanomaßstab herstellen, die leicht durch ihre rubinrote Farbe erkennbar sind. Ein Weg, Nanogold herzustellen, ist die Citratmethode, die hier beschrieben ist. Damit kann man entweder kolloidales Gold oder Goldcluster in Lösung herstellen.
Ein Cluster, oder Nanopartikel, ist ein Verbund von 3 bis 50 000 Atomen. Üblicherweise liegt der Durchmesser von Gold-Nanopartikeln zwischen 12-18 nm. Sind die Cluster räumlich in einem anderen physikalischen Medium verteilt, dann spricht man von einem kolloidalen System.
Mit freundlicher Genehmigung von Nicola Graf
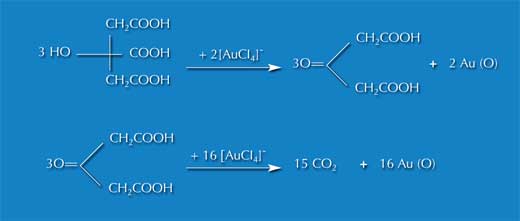
Das Experiment basiert auf einer Redoxreaktion von Goldtetrachlorid (auch bekannt als Tetrachlorogoldsäure oder Tetrachlorgoldsäure (III)-Trihydrat), bei dem die Goldionen zu atomaren Goldclustern reduziert werden. Das Reduktionsmittel Natriumcitrat (auch Trinatriumcitrat-Dihydrat genannt) reduziert nicht nur Gold, sondern wirkt auch als Dispersionsmittel, welches die gebildeten Goldcluster stabilisiert.
Durch die Zugabe des Reduktionsmittels wird die Zusammenlagerung der Metallionen gestoppt und das Ergebnis ist ein kolloidales Cluster, eingeschlossen in ein Ligandengehäuse.
Diese Kolloide werden durch den Tyndall-Effekt nachgewiesen. Dieser tritt ein, wenn Licht durch eine kolloidale Flüssigkeit fällt: Den Weg des Lichts kann man sehen, wenn sichtbares Licht durch supendierte, mikroskopisch kleine Partikel mit einem Durchmesser in der Größenordnung der Wellenlänge des sichtbaren Lichtes (400-800 nm) gestreut wird. Im Gegensatz dazu ist der Weg des Lichts durch eine Flüssigkeit ohne Kolloide (z.B. Tinte) nicht erkennbar, weil das Licht ohne Streuung durchgeht.
Materialien
- Goldchloridlösung, HAuCl4 (0,1 g Goldchlorid in 20 ml H2O)
- Citratlösung, C6H5Na3O7 x 2 H2O (5,7 g in 0,5 L H2O, gefiltert)
- Destilliertes Wasser
- Kochplatte oder Tauchsieder
- Rührgerät (Löffel, Rührer oder ähnliches), idealerweise ein Magnetheizrührer
- 1 hitzestabiler Glasbecher (50-100 ml)
- Thermometer (bis 100 °C)
- Laserpointer (optional)
Sicherheitshinweis: Goldchlorid ist ätzend und gesundheitsschädlich beim Verschlucken.
Vorgehen
- Zu 28 ml destilliertem Wasser gibt man 0,5 ml (das sind etwa 15 Tropfen) Goldchloridlösung.
- Die Lösung auf dem Rüher oder der Kochplatte auf 100 °C erhitzen.
- Erreicht die Lösung eine Temperatur von 100 °C und fängt an zu sprudeln, gibt man so schnell wie möglich 1,5 ml Citratlösung zu und rührt heftig.
Die anfänglich rote Farbe der Goldchloridlösung intensiviert sich bis tiefrot. Bei Temperaturen zwischen 85 und 90 °C, dauert es etwa 5 Minuten bis sich die Farbe ändert; bei 100 °C geht es noch schneller.
Abhängig von der Größe der gebildeten Partikel kann die Farbe violett statt rot werden.
- Die Goldkolloide erkennt man am Tyndall-Effekt. Leuchten Sie mit dem Laserpointer von der Seite durch die Lösung. Der Lichtweg durch die Lösung ist erkennbar.
Weitere Experimente
Wiederholen Sie das Experiment zum Vergleich mit 0,5 ml Goldchloridlösung und 50 ml destilliertem Wasser. Vergleichen Sie die Zeit bis zur Farbänderung.
Wenn man in einem weiteren Experiment die Citratkonzentration erhöht, erzeugen die Kolloide einen violetten Farbton, das Ergebnis der Bildung einer anderen Kolloidgröße.
Weitere Informationen:
Für weitere Informationen nehmen Sie bitte Kontakt auf mit NanoBioNet e.V.: www.nanobionet.de
Email: info@nanobionet.de
Tel: +49 (0)681 685 7364
Web References
- w1 – Die deutschsprachige Webseite der Saarlab-Initiative finden Sie unter: www.saarlab.de
- w2 – Die Webseite für Ecsite, das europäische Netzwerk der Wissenschaftszentren, können Sie finden unter: www.ecsite.net
- w3 – Die nanoTruck-Webseite (auf deutsch oder englisch) können Sie aufrufen unter: www.nanotruck.de
- w4 – Für weitere Informationen über Nanowissenschaft aus der Universität Cambridge siehe: www.nanoscience.cam.ac.uk/schools
- w5 – Für eine Liste nützlicher Links zur Nanotechnologie für Schulen siehe: www.nanoscience.cam.ac.uk/schools/links.html
- w6 – Die Webseite von NanoBioNet e.V. finden Sie unter: www.nanobionet.de
- w7 – Für weitere Informationen zur NanoSchoolBox siehe: www.nanobionet.de/12105_11931.htm
- w8 – Ferrofluide können bei FerroTec GmbH bestellt werden: www.ferrofluid.de
- w9 – Für weitere Informationen über Nano2Life, dem ersten europäischen Exzellenznetzwerk der Nanobiotechnologie, siehe: www.nano2life.org
Resources
- Capellas Espuny M (2003) Renaissance artists decorated pottery with nanoparticles. ESRF Newsletter 38: 4-5. www.esrf.eu/UsersAndScience/Publications/Newsletter
Review
Obwohl Nanotechnologie ein Modewort ist, von Europäern positiv eingeschätzt (siehe Eurobarometer-Umfrage 2005), hat Nanotechnologie für die meisten Leute, einschließlich Studenten, eine eher futuristische denn reale Bedeutung.
Matthias Mallmanns Artikel, der mit alten, gefärbten Glasfenstern beginnt, geht das Thema auf liebenswürdige Weise an. Er spannt den Bogen von möglichen Quellen in Europa für den Nanotechnologieunterricht zu didaktischem Material (NanoSchoolBox) mit der Möglichkeit zu eigenen Experimenten.
Diesen Artikel empfehle ich Lehrern der oberen Sekundarstufe im Wissenschaftsunterricht, die Nanotechnologie im Rahmen von realen Anwendungen einführen wollen. Das Material eignet sich auch für Studenten, die ihr Verständnis des Themas mittels der zitierten Webseiten vertiefen wollen.
Stil und Niveau der Einzelheiten eignen sich für nicht-englische Muttersprachler, vorausgesetzt sie haben einen wissenschaftlichen Hintergrund. Mit den beschriebenen Beispielen und Vorschlägen können unterschiedliche Wissenschaftsbereiche (Physik, Chemie, Biologie) miteinander verbunden werden oder die Aktivitäten auf geschichtliche oder Aspekte aktiver Bürgerbeteiligung (Sicherheitsthemen) ausgeweitet werden.
Giulia Realdon, Italien
